La méthode mise au point par des chercheurs de l’Institut Européen des Membranes de Montpellier pour analyser la structure du cyclobutadiène, une molécule organique particulièrement instable, ouvre la voie au contrôle de la réactivité d’autres molécules, rendant ainsi possibles des réactions chimiques actuellement impossibles. Explications.
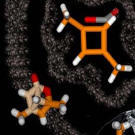
Quelques molécules organiques sont par nature instables. C’est le cas du cyclobutadiène pour lequel les chimistes théoriciens prédisent une ultra-réactivité surprenante qui se vérifie expérimentalement. Une fois le cyclobutadiène synthétisé, il se combine instantanément avec lui-même (dimérisation) ou avec d’autres molécules proches. Constitué de 4 atomes de carbone et de 4 atomes d’hydrogène, les théories prédisent une structure carrée ou rectangulaire : chaque carbone, positionné à un sommet du carré, est lié à un atome d’hydrogène.
Depuis les années 60, plusieurs équipes de chercheurs ont réussi à stabiliser suffisamment longtemps cette molécule dans des matrices d’argon à très basse température pour mesurer les spectres de vibration. Ensuite, plusieurs stratégies utilisant par exemple des ions métalliques interagissant avec la molécule ont augmenté son temps de vie de quelques millisecondes à plusieurs heures.
Donald J. Cram, prix Nobel de chimie en 1987 (avec J.-M. Lehn et Ch. J. Pedersen), stabilise le cyclobutadiène in-situ dans un conteneur moléculaire où il ne peut ni réagir avec lui-même, ni être en contact avec d’autres molécules réactives. Les spectres de Résonance Magnétique Nucléaire donnant des indications sur la structure sont alors enregistrés. Hélas, le caractère trop désordonné des conteneurs moléculaires empêche la détermination directe de la structure cristallographique du cyclobutadiène par diffraction des rayons.
Des chercheurs de l’équipe « Nanosystèmes Supramoléculaires Adaptatifs » de l’Institut Européen des Membranes (CNRS / Université de Montpellier II / Ecole Nationale Supérieure de Chimie de Montpellier), conduits par Mihail Barboiu ont choisi l’auto-organisation supramoléculaire pour construire de nouvelles architectures synthétiques cristallines, de structures et de dimensions adaptées au piégeage du cyclobutadiène, ne perturbant pas l’analyse aux rayons X. Les structures carrée et rectangulaire de cette molécule particulièrement instable ont ainsi pour la première fois été révélées par les rayons X.
Grâce à cette méthode, on peut maintenant envisager de stabiliser d’autres molécules très instables en choisissant la matrice adaptée. On pourra alors contrôler la réactivité de ces molécules rendant possibles d’autres réactions chimiques actuellement inenvisageables.



















Réagissez à cet article
Vous avez déjà un compte ? Connectez-vous et retrouvez plus tard tous vos commentaires dans votre espace personnel.
Inscrivez-vous !
Vous n'avez pas encore de compte ?
CRÉER UN COMPTE