Présentation
Auteur(s)
-
Jean CAVARELLI : Professeur de Biologie structurale, université Louis-Pasteur, Strasbourg
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
Les molécules biologiques responsables de toute vie cellulaire sont des hétéropolymères de très grande taille appartenant à deux familles : les protéines et les acides nucléiques. Les processus biologiques compliqués sont les résultats d’interactions dynamiques soit de macromolécules biologiques entre elles, soit de macromolécules avec de petits substrats cellulaires. La compréhension de ces mécanismes nécessite en premier lieu la connaissance des structures tridimensionnelles de ces macromolécules soit seules, soit engagées dans des complexes spécifiques. La connaissance de ces structures est l’un des piliers actuels de la biologie moléculaire et représente une source de progrès qui génère des retombées non seulement en recherche fondamentale mais aussi en recherche appliquée (médicale, agroalimentaire). Cela justifie les investissements importants réalisés depuis plusieurs années dans les secteurs publics et privés. La diffraction des rayons X par des monocristaux est la méthode par excellence pour l’étude des macromolécules biologiques. La cristallographie a permis la détermination des structures tridimensionnelles de plusieurs milliers de macromolécules biologiques dans des gammes de taille et de complexité très variées : petites protéines, oligonucléotides, acides ribonucléiques de transfert, immunoglobulines complexes multienzymatiques, complexes nucléoproté-iques, virus d’insectes, de plantes ou de mammifères. Les propriétés physico-chimiques intrinsèques des macromolécules biologiques donnent naissance à des cristaux avec de grands paramètres de maille cristalline et un pouvoir de diffraction en général limité en comparaison du standard actuel des petites molécules organiques. Cela impose des méthodes et des techniques adaptées tout au long du processus cristallographique. Cette méthodologie propre aux macromolécules biologiques va être présentée dans cet article. L’explosion actuelle de cette méthode est due aux progrès réalisés tant au niveau de la technologie (biologie moléculaire, sources de rayons X, détecteurs de rayons X, supercalculateurs puissants) qu’au niveau des logiciels de traitement des données de diffraction (collecte, phasage, affinement). Cela se traduit par un raccourcissement extraordinaire du délai séparant l’obtention d’un premier cristal et la détermination de la structure cristalline. Une étude cristallographique peut maintenant être conduite en quelques mois après l’obtention des premiers cristaux.
La lecture de cet article suppose une bonne connaissance de la cristallographie géométrique et une première initiation à la théorie de la diffraction des rayons X par des monocristaux. Le lecteur pourra se référer aux articles de A. Authier « Cristallographie géométrique » dans le traité de Sciences Fondamentales [1] et de Y. Jeannin « Résolution d’une structure cristalline par rayons X » dans ce traité Analyse et Caractérisation [3].
DOI (Digital Object Identifier)
Cet article fait partie de l’offre
Bioprocédés et bioproductions
(158 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Un Parcours Pratique
Opérationnel et didactique, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive
Présentation
7. Remplacement moléculaire
Le terme de remplacement moléculaire représente une famille de techniques dont l’objet est d’utiliser la présence d’une macromolécule, d’une sous-unité de macromolécule, ou d’un fragment de macromolécule, dans différents environnements cristallographiques, pour déterminer ou améliorer des phases initiales. C’est la méthode de choix lorsque la macromolécule à étudier est parente à une autre, dont la structure tridimensionnelle est connue. Ce qui est important ici est la parenté structurale, c’est-à-dire la similitude du repliement tridimensionnel. Cette similarité structurale est en général mise en évidence par des méthodes d’analyse des séquences. La méthode du remplacement moléculaire n’utilise que les modules des facteurs de structures de la protéine native sans nécessiter l’ajout d’atomes lourds supplémentaires. Pour utiliser cette méthode, on doit disposer :
-
d’un espace complet de diffraction pour la molécule X dont on cherche à déterminer la structure tridimensionnelle ;
-
de la structure d’une molécule M que l’on suppose être parente à X, c’est-à-dire que les deux molécules sont supposées avoir un repliement tridimensionnel commun (partiellement ou complètement).
La méthode du remplacement moléculaire utilise les propriétés de la fonction de Patterson qui est le produit de convolution de la densité électronique par son image obtenue par un centre de symétrie par rapport à l’origine :
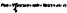
avec :
- ρ (r ) :
- densité électronique en un point M de la maille repéré par le vecteur r
- V :
- volume de la maille cristalline.
On peut montrer que les maxima de la fonction de Patterson correspondent aux vecteurs interatomiques. Ces vecteurs peuvent être schématiquement divisés en deux classes :
-
les vecteurs intramoléculaires, reliant deux atomes de la même molécule (ou d’une même sous-unité). Ces vecteurs...
Cet article fait partie de l’offre
Bioprocédés et bioproductions
(158 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Un Parcours Pratique
Opérationnel et didactique, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive
Remplacement moléculaire
Cet article fait partie de l’offre
Bioprocédés et bioproductions
(158 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Un Parcours Pratique
Opérationnel et didactique, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive