Présentation
Auteur(s)
-
Boyan MUTAFTSCHIEV : Directeur de Recherche au CNRS, Laboratoire Maurice Letort, Villers-lès-Nancy
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
Cet article traite les phénomènes ayant lieu à l’interface entre un solide et son milieu, à l’équilibre et en cas de croissance du solide. Le trait commun est la rencontre, à l’interface, de deux flux de matière de sens opposés : l’un, constitué de molécules qui s’y déposent avant d’être incorporées dans le réseau cristallin, l’autre, de molécules qui quittent l’interface en direction du milieu. À l’équilibre, l’intensité des deux flux est égale et dépend de la cinétique interfaciale, elle-même régie par les propriétés des phases au voisinage immédiat de l’interface. À la sursaturation, représentée par la différence des potentiels chimiques dans les deux phases, le flux de croissance est prédominant, sans qu’il existe cependant une dépendance linéaire entre le flux net et la sursaturation, comme l’on aurait pu s’y attendre par analogie avec l’électrodynamique en assimilant l’interface à une résistance passive.
La voie que nous nous proposons de suivre passe donc par la considération des équilibres à l’interface entre un cristal et son milieu, qui nous révèlent les mécanismes microscopiques à la saturation, avant d’aborder la cinétique interfaciale de croissance, dont la dépendance avec la sursaturation peut être assez complexe. Deux remarques découlent de cette procédure.
— L’approche utilisée est exclusivement moléculaire-statistique. Par rapport à l’approche basée sur la thermodynamique classique et sur la mécanique des milieux continus , la méthode choisie a l’avantage de mieux visualiser les phénomènes physiques, au prix de quelques concessions à la rigueur mathématique. En outre, elle s’avère mieux adaptée au traitement des systèmes à énergie de surface élevée et fortement anisotrope, tel un cristal qui croît à partir de sa vapeur.
— Il faut souligner que la cinétique globale de croissance dépend autant de la cinétique interfaciale que de la cinétique du transport de matière du milieu vers l’interface. Cependant, les mécanismes du transport dans le volume sont communs à d’autres procédés (génie chimique, combustion, etc.) et sont traités en détail par la mécanique des fluides, d’où notre choix de ne pas dépasser dans cet article le cadre des phénomènes interfaciaux.
DOI (Digital Object Identifier)
Cet article fait partie de l’offre
Physique Chimie
(200 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Un Parcours Pratique
Opérationnel et didactique, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive
Présentation
1. Équilibre des phases
1.1 Rappels de thermodynamique, phénoménologique et statistique
Un système hétérogène est composé de phases séparées par des interfaces. À l’équilibre et en absence d’une force extérieure, la valeur de toute grandeur thermodynamique est constante dans n’importe quel point d’une phase. Aux interfaces, un bon nombre de propriétés peuvent changer d’une façon plus ou moins abrupte, telles la densité de matière, l’énergie d’interaction entre molécules, l’entropie, etc., alors que d’autres, tels le potentiel chimique ou la température, ne varient pas.
Le potentiel chimique
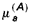 d’un composé a dans une phase A est défini comme le travail qu’il faut faire sur le système pour que le nombre de molécules dans cette phase augmente de
d’un composé a dans une phase A est défini comme le travail qu’il faut faire sur le système pour que le nombre de molécules dans cette phase augmente de
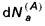 , tout autre paramètre d’état étant constant. Si l’énergie libre du système est F, il vient :
, tout autre paramètre d’état étant constant. Si l’énergie libre du système est F, il vient :
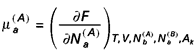 ( 1 )
( 1 )
avec
-
b ¹ a et B ¹ A,
-
Ttempérature thermodynamique,
-
Vvolume,
-
Akaire de la k ième interface.
La tension de surface γ k de la k ième interface est définie comme le travail fait sur le système quand l’aire de l’interface augmente de dAk , tout autre paramètre d’état étant constant :
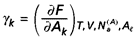
Cet article fait partie de l’offre
Physique Chimie
(200 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Un Parcours Pratique
Opérationnel et didactique, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive
Équilibre des phases
BIBLIOGRAPHIE
-
(1) - NOZIÈRES (P.) - * - Cours de croissance cristalline au Collège de France, Paris, (non publié) (1984).
-
(2) - STERN (O.) - Zur kinetischen Theorie des Dampfdrucks einatomiger fester Stoffe und über die Entropie-Konstante einatomiger Gase. - Physik Z. (Allemagne) 14, 629 (1913).
-
(3) - HENDERSON (D.), BARKER (J.A.) - Perturbation Theories. - Physical Chemistry – An Advanced Treaties. Eyring (H.), Henderson (D.) et Jost (W.) ed., vol. VIIIA, Acad. Press, NY (États-Unis), p. 377-412 (1971).
-
(4) - STRANSKI (I.N.) - Zur Theorie des Kristallwachstums. - Z. physik Chem. (Allemagne) 136, 259 (1928).
-
(5) - KOSSEL (W.) - Zur Theorie des Kristallwachstums. - Nachrichten der wissenschaftlichen Gesellschaft Göttingen (Allemagne) 135 (1927).
-
(6) - KAISCHEW (R.) - Über die elementaren Anlagerungs – und...
Cet article fait partie de l’offre
Physique Chimie
(200 articles en ce moment)
Cette offre vous donne accès à :
Une base complète d’articles
Actualisée et enrichie d’articles validés par nos comités scientifiques
Des services
Un ensemble d'outils exclusifs en complément des ressources
Un Parcours Pratique
Opérationnel et didactique, pour garantir l'acquisition des compétences transverses
Doc & Quiz
Des articles interactifs avec des quiz, pour une lecture constructive