Présentation
Auteur(s)
-
Bernard WEBER : Docteur ès Sciences Physiques - Directeur de Recherche au Centre National de la Recherche Scientifique (CNRS) (Laboratoire d’Études et de Recherches en Mécanique et Énergétique des Surfaces)
-
Jean-Jacques EHRHARDT : Docteur ès Sciences Physiques - Directeur de Recherche au CNRS (Laboratoire Maurice Letort)
-
André THOMY : Docteur ès Sciences Physiques - Directeur de Recherche au CNRS (Laboratoire commun CNRS Saint-Gobain, Unité Mixte 37)
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
Le domaine des surfaces revêt une importance particulière car tout corps, liquide ou solide, interagit avec le milieu ambiant à travers la surface qui le délimite. Or les atomes se trouvant à la surface d’un solide ou d’un liquide présentent une coordinence moins importante que ceux situés au cœur de ce système ; on conçoit donc que ces atomes vont conférer à la surface des propriétés tout à fait spécifiques. Ainsi, l’énergie nécessaire pour augmenter la surface d’un solide est toujours positive, ce qui a pour conséquences, entre autres, que les systèmes condensés ont tendance, pour minimiser leur énergie libre de surface, à diminuer l’étendue de cette surface, à réagir avec les molécules de l’atmosphère ambiante pour former une couche dite d’adsorption ou, par exemple, à faire ségréger en surface l’élément du solide qui a la plus faible énergie superficielle.
Ces propriétés particulières donnent aux systèmes dispersés un rôle important dans des domaines très divers de la physique, de la chimie mais aussi de la géologie et de la biologie. Ainsi, certaines réactions chimiques, thermodynamiquement possibles, sont accélérées, ou sont favorisées quand elles sont en compétition avec d’autres réactions également possibles, grâce à la surface de certains solides ; ce phénomène, la catalyse hétérogène, revêt une importance cruciale, par exemple en pétroléochimie. Des remarques analogues pourraient être faites dans les domaines de la métallurgie, de l’électronique, de la croissance cristalline, de l’adhésion et de la rupture des solides, de la lubrification, de la corrosion, etc.
L’importance de ces phénomènes superficiels a d’ailleurs été comprise très tôt ; ainsi, J. W. Gibbs a développé la thermodynamique des surfaces à la fin du siècle dernier ; de même, un grand nombre de travaux de I. Langmuir, dans le domaine de l’adsorption et de la cinétique chimique hétérogène, n’ont pas perdu de leur actualité bien qu’ils datent du début de ce siècle. Cependant, malgré quelques exceptions importantes, les études expérimentales sur surfaces bien contrôlées furent rares avant les années soixante-dix. Au cours de cette décennie, ces recherches ont pu commencer dans de bonnes conditions grâce au développement de l’ultravide (favorisé par la recherche spatiale). Des pressions inférieures à 10 – 8 Pa sont en effet nécessaires pour éviter la contamination des surfaces, la réactivité de ces dernières étant généralement très forte (analogue à celle de radicaux libres). À la suite de cela, la mise au point de techniques spécifiques a permis d’étudier la structure (diffraction d’électrons lents) et la composition superficielle (spectrométrie d’électrons Auger).
Nous avons donc affaire à un secteur en plein développement qui rassemble des scientifiques d’horizons très divers (des métallurgistes, des physico-chimistes, des physiciens du solide, des électroniciens, des électrochimistes, etc.) et qui trouve des applications dans ces différents domaines. Cet article traite plus particulièrement de l’adsorption et de la ségrégation. Pour un panorama général de ces phénomènes et de leurs applications, on pourra consulter les ouvrages cités en documentation .
VERSIONS
- Version courante de févr. 1990 par Boyan MUTAFTSCHIEV
DOI (Digital Object Identifier)
Présentation
Article inclus dans l'offre
"Physique Chimie"
(205 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
3. Thermodynamique des surfaces
Les interfaces posent des problèmes thermodynamiques tout à fait spécifiques, car à leur existence propre est liée une énergie dont la définition précise (et plus encore la mesure expérimentale) présente des difficultés. Bien que J. W. Gibbs ait déjà attiré l’attention sur certains de ces problèmes particuliers, plusieurs points importants ne sont pas encore entièrement élucidés ; il en est ainsi, en particulier, des notions de tension, de contrainte, d’énergie superficielle, etc. L’identité ou au contraire la différence entre certaines de ces grandeurs n’est pas toujours claire et même les notations, différentes d’un ouvrage à l’autre, posent de sérieux problèmes ). Il conviendra donc, toujours, de bien se reporter aux définitions de chacune des grandeurs lors de la consultation d’un article.
Dans ce paragraphe seront décrites des situations d’équilibre, ce qui n’est bien sûr pas forcément le cas dans la pratique, en particulier pour la ségrégation quand la barrière de diffusion ne peut être franchie. On débutera par un rappel de thermodynamique des phases volumiques (quand la présence des surfaces est ignorée ou négligée) de manière à introduire les grandeurs classiques et à préciser les notations dont on généralisera les définitions et les applications par la suite, quand l’existence des surfaces sera prise en compte.
3.1 Fonctions thermodynamiques et relations générales
Rappelons que, quand on néglige l’effet des surfaces et en l’absence de tout champ de force (électrique, magnétique, gravitationnel, etc.), la variation d’énergie interne, qui accompagne toute évolution réversible (δQ = T dS ) d’un système constitué de plusieurs phases en équilibre sur lequel les contraintes mécaniques appliquées sont purement hydrostatiques (δW = – p dV ), est :
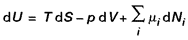
Thermodynamique des surfaces
Article inclus dans l'offre
"Physique Chimie"
(205 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
BIBLIOGRAPHIE
-
(1) - BEVER (M.B.) - Encyclopedia of materials science and engineering - (8 volumes). New York Pergamon Press (contient de très nombreux articles sur les surfaces, l’adsorption, la ségrégation et les applications) (1986).
-
(2) - SOMORJAI (G.A.) - Chemistry in two dimensions. Surfaces. - Ithaca, Cornell University Press (1981).
-
(3) - BERTHIER (Y.), DELAMARE (F.), HONDROS (E.), HUBER (M.), MARCUS (P.), MASSON (A.), OUDAR (J.), RHEAD (G.E.) - Adsorption on metal surfaces, an integrated approach. - Amsterdam, ed. BENARD (J.) Elsevier Sci. Publ. Co (1983).
-
(4) - ERTL (G.), KUPPERS (J.) - Low energy electrons and surface chemistry. - Weinheim Verlag Chemie (1985).
-
(5) - OTHANI (H.), KAO (C.T.), VAN HOVE (M.A.), SOMORJAI (G.A.) - A tabulation and classification of the structures of clean solid surfaces and of adsorbed atomic and molecular monolayers as determined from low energy electron diffraction patterns. - Progress in Surface Science (USA), 23, p. 155-316 (1986).
-
...
Article inclus dans l'offre
"Physique Chimie"
(205 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.




