Présentation
Auteur(s)
-
Paul de MOLLIENS : Ancien Directeur Technique de la Société Cofaz
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
La conversion du monoxyde de carbone par la vapeur d’eau constitue une étape essentielle de la production d’hydrogène à partir de sources carbonées (charbon) ou hydrocarbonées (pétrole, gaz naturel) préalablement transformées par oxydation en gaz de synthèse (CO + H2 ), l’agent oxydant étant soit de l’oxygène (craquage autothermique), soit de la vapeur d’eau (reformage catalytique).
DOI (Digital Object Identifier)
Présentation
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
1. Bases thermodynamiques
La conversion du monoxyde de carbone par la vapeur d’eau s’effectue en phase gazeuse par la réaction chimique réversible :
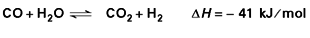
La réaction étant équimolaire, l’équilibre n’est pas influencé par la pression dans les conditions industrielles courantes (entre la pression atmosphérique et 50 bar, soit 5 MPa).
La conversion étant assez fortement exothermique, l’équilibre est déplacé à haute température vers la formation d’oxyde de carbone, et à basse température vers la formation d’hydrogène.
Dans les conditions de température élevée (950 à 1 500 oC) où s’opère la production de gaz de synthèse en présence de vapeur d’eau, l’équilibre de la réaction de conversion est pratiquement atteint, la teneur en oxyde de carbone étant d’autant plus importante que la température est élevée, toutes choses égales par ailleurs.
Inversement, on favorise la production d’hydrogène par un abaissement de la température et / ou par un appoint de vapeur d’eau. À température plus basse, l’abaissement de la vitesse de réaction est tel qu’il convient d’utiliser des catalyseurs afin d’obtenir des cinétiques acceptables.
-
Expression de la constante d’équilibre : des considérations thermodynamiques ont permis de proposer des équations permettant de déterminer la valeur de la constante d’équilibre en fonction de la température. Une formule approchée valable à la pression atmosphérique est la suivante :
lg K = 2 059 T – 1 – 1,590 4 lg T + 1,817 × 10 – 3 T – 5,65 × 10 –7 T 2 + 8,24 × 10 –11 T 3 + 1,531 3( 1 )avec :
- T (K) :
- température.
Bases thermodynamiques
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.




