Présentation
Auteur(s)
-
Didier DEVILLIERS : Docteur ès Sciences - Professeur à l’Université Pierre-et-Marie Curie, Paris
-
Marius CHEMLA : Professeur à l’Université Pierre-et-Marie Curie, Paris - Directeur du Laboratoire d’Électrochimie
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
Avant d’aborder la cinétique électrochimique, il convient de faire quelques rappels de thermodynamique. En effet, la notion de surtension, par exemple, exige la connaissance des potentiels d’électrode à l’équilibre. Ces derniers sont mesurables par rapport à une électrode de référence ; aussi, avons-nous jugé utile de rappeler les principales électrodes de référence les plus utilisées en milieu aqueux.
Il nous a paru également nécessaire de donner les définitions précises des grandeurs couramment utilisées en cinétique électrochimique. Les données numériques situées en fin d’article sont précédées d’un mode d’emploi de façon à faciliter leur utilisation.
Enfin, nous avons répertorié quelques applications particulièrement importantes de la connaissance des grandeurs cinétiques.
Alors qu’un tableau des potentiels standards peut quasiment être exhaustif dans la mesure où il est possible de recenser, pour un milieu et une température donnés, la plupart des couples rédox possibles (si l’on excepte les composés organiques, très nombreux), ce ne sera jamais le cas en cinétique car les grandeurs mises en jeu dépendent du milieu, de la température et parfois des concentrations, mais aussi et surtout, de la nature et de la structure du matériau d’électrode. Aussi, dans les tableaux qui suivront, avons-nous fait un choix forcément arbitraire. Toutefois, même si le lecteur ne trouve pas mention dans ces tableaux des grandeurs qu’il recherche, la lecture du mode d’emploi lui sera utile pour éviter certains écueils liés à l’interprétation et à l’utilisation des données de la littérature.
Sauf indication contraire, les grandeurs cinétiques regroupées ci-après sont extraites de l’Encyclopédie de l’Électrochimie des éléments . Le lecteur est invité à se référer à cet ouvrage très complet pour plus d’informations sur un élément particulier. En ce qui concerne les composés organiques, il pourra consulter l’ouvrage de Baizer .
VERSIONS
- Version courante de juin 2015 par Didier DEVILLIERS
DOI (Digital Object Identifier)
Présentation
Article inclus dans l'offre
"Corrosion Vieillissement"
(98 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
2. Applications
2.1 Domaine d’électroactivité
L’oxydation et la réduction du solvant ou de l’électrolyte-support constituent deux barrières au-delà desquelles aucune étude n’est possible. La plage de potentiel entre ces deux bornes constitue le domaine d’électroactivité du milieu. Compte tenu du domaine thermodynamique de stabilité de l’eau, la largeur du domaine d’électroactivité de ce solvant devrait être égale à 1,23 V quel que soit le pH. La plage de potentiel utilisable dépend notamment de la cinétique du dégagement d’oxygène et d’hydrogène. Cette cinétique est tributaire du matériau de l’électrode ; le domaine d’électroactivité de l’eau est en fait toujours plus large que 1,23 V (environ 1,7 V sur électrode de platine). En jouant sur les facteurs qui déterminent le domaine d’électroactivité (solvant, électrolyte-support, matériau de l’électrode), on peut choisir les conditions opératoires adaptées à l’étude d’un couple rédox particulier.
HAUT DE PAGE2.2 Polarographie
La surtension de dégagement d’hydrogène est très importante sur cathode de mercure en milieu aqueux. Dépendant du pH, elle est particulièrement élevée avec les électrolytes neutres. L’élargissement de la plage des potentiels négatifs ainsi explorables sur ce type d’électrode permet l’étude quantitative de nombreuses vagues cathodiques. Cette technique électrochimique d’analyse, appelée polarographie, a été mise au point en 1921 par Heyrovsky. Elle est encore utilisée de nos jours, avec divers perfectionnements qui ont permis d’accroître sa précision (polarographie à impulsions surimposées). Dans les tableaux 6 et 7 sont recensés quelques potentiels de demi-vague obtenus sur électrode à goutte de mercure.
La plage de potentiel est limitée du côté anodique par l’oxydation du mercure en
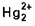 vers + 0,3 V/ ENH ou par la formation de sels mercureux...
vers + 0,3 V/ ENH ou par la formation de sels mercureux...
Applications
Article inclus dans l'offre
"Corrosion Vieillissement"
(98 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
BIBLIOGRAPHIE
-
(1) - * - * étude théorique de la question
-
(2) - * - □ description d’appareillages ou d’installations
-
(3) - * - Δ comporte des résultats d’essais de laboratoire
-
(4) - * - △ comporte des résultats pratiques ou industriels
-
(5) - BARD (A.J.), éd - Encyclopedia of Electrochemistry of the Elements - (Encyclopédie de l’Électrochimie des Éléments). Volume IX-A, 612 p., M. Dekker, 270 Madison Avenue NEW YORK NY 10016, USA (1982) (* △).
-
(6) - BARD (A.J.), éd - Encyclopedia of Electrochemistry of the Elements - (Encyclopédie de l’Électrochimie des Éléments). Volume II, 515 p., M. Dekker, 270 Madison Avenue NEW YORK NY 10016, USA (1974) (* △).
-
...
Article inclus dans l'offre
"Corrosion Vieillissement"
(98 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.