Présentation
Auteur(s)
-
Pierre VITORGE : Ingénieur au Commissariat à l’énergie atomique (CEA) à Saclay
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
Cet article présente les bases fondamentales de la chimie des actinides, décrit ensuite qualitativement les principales parties du cycle du combustible et se termine avec des données quantitatives.
Les rappels théoriques donnent des notions qualitatives pour expliquer la réactivité chimique des actinides et comprendre ainsi les valeurs des grandeurs thermodynamiques qui permettent des prévisions quantitatives à l’équilibre. La banque de données thermodynamiques (Thermodynamic Data Base, TDB) de l’Agence pour l’Énergie Nucléaire (AEN-OCDE) et en France le CEA (Commissariat à l’Énergie Atomique) en ont récemment évalué certaines en utilisant et développant des méthodologies dont nous présentons ici certains aspects.
Nous décrirons quelques problèmes d’actualité où la chimie des actinides joue un rôle central : évaluation des possibilités d’améliorer le recyclage (retraitement) des actinides à vie longue, de prévoir leur comportement dans l’environnement pour comparer l’impact des différentes options de gestion des déchets.
Les diagrammes de Pourbaix résument la chimie en solution, nous y avons ajouté des indications sur la solubilité, l’influence de la force ionique et de la complexation en milieux bicarbonate /carbonate (
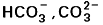 ). La discussion du choix des constantes d’équilibre est l’occasion d’attirer l’attention sur les points délicats et de souligner les zones d’ombre, les incertitudes et les données à confirmer.
). La discussion du choix des constantes d’équilibre est l’occasion d’attirer l’attention sur les points délicats et de souligner les zones d’ombre, les incertitudes et les données à confirmer.
VERSIONS
- Version courante de août 2021 par Thomas VERCOUTER
DOI (Digital Object Identifier)
Présentation
Article inclus dans l'offre
"Génie nucléaire"
(171 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
5. Données thermodynamiques en milieux hydroxyde et carbonate
Les milieux aqueux hydroxyde, carbonate et bicarbonate ont été les plus étudiés récemment en raison de leur importance dans l’environnement. Les constantes d’équilibre des actinides courants sont suffisamment bien connues pour des prévisions raisonnables de leur comportement dans de nombreuses conditions (Chimie des actinides[Form. BN 3 520], figures 1 à 13) ; par contre, la validation des données reste partielle et leur précision est parfois insuffisante pour les vérifications expérimentales d’exercices de modélisation. Les valeurs des constantes d’équilibres (Chimie des actinides[Form. BN 3 520], tableaux 2 à 6) sont choisies et souvent recalculées à partir des résultats originaux lors de revues critiques [13, 14, 18, 31] qui permettent aussi d’identifier les laboratoires les plus fiables. Outre les erreurs classiques (mauvaise interprétation, manque de précision, transformation de la phase solide en cours de mesure de solubilité...), les écarts entre résultats publiés viennent souvent d’un mauvais étalonnage de l’électrode de référence lors de mesures de pH ou électrochimiques, dû à une prise en compte incorrecte du potentiel de jonction et des coefficients d’activité. Il faut imposer la même force ionique avec le même sel de fond dans la solution de travail et les étalons et, si possible, dans la solution de l’électrode de référence [26]...
Données thermodynamiques en milieux hydroxyde et carbonate
Article inclus dans l'offre
"Génie nucléaire"
(171 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
Article inclus dans l'offre
"Génie nucléaire"
(171 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.