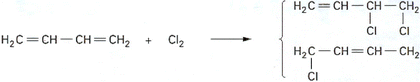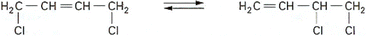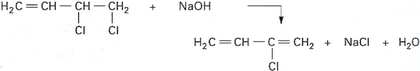Présentation
Auteur(s)
-
Jean-Louis LOCATELLI : Ancien responsable Recherche et développement EniChem Élastomères France
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
Si, historiquement, la découverte et le développement du polychloroprène ont été liés à la synthèse du monomère par la voie acétylène, seule, aujourd’hui, la synthèse à partir du butadiène est industriellement pratiquée.
Le présent article décrit successivement les différentes étapes de fabrication du chloroprène monomère, puis sa polymérisation en émulsion (principe, mécanismes réactionnels, procédé industriel). Ensuite sont présentées les techniques de coagulation du latex et d’isolation du caoutchouc, la structure des différents polychloroprènes modifiés au soufre et au mercaptan, leur mise en œuvre et leurs propriétés à l’utilisation.
DOI (Digital Object Identifier)
Présentation
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
2. Obtention des matières premières
2.1 Chloroprène
La synthèse industrielle du chloroprène est réalisée en trois étapes successives :
-
chloration du butadiène pour former des dichlorobutènes :
![]()
-
isomérisation de ces chlorobutènes en dichloro-3,4-butène-1 :
![]()
-
déshydrochloration du dichlorobutène pour former le chloroprène :
![]()
-
La première étape, chloration du butadiène, est effectuée en phase gazeuse à des températures voisines de 250 oC et en présence d’un excès de butadiène.
Les réactions de formation des dichlorobutènes sont d’ordre 1 par rapport au chlore et au butadiène. Les énergies d’activation des deux chlorobutènes (-3,4- et -1,4-) sont pratiquement égales (54,4 kJ/mol).
La réaction de chloration est fortement exothermique (ΔH = – 184 kJ/mol) et spontanée (ΔG = – 142,3 kJ/mol). Le rapport molaire butadiène/chlore est voisin de 10, ce qui correspond à un taux de conversion maximal du butadiène de 10 à 12 %, l’excès servant de volant thermique.
La réaction s’effectue dans un réacteur piston, en partant de gaz réactifs prémélangés à haute vitesse, sous une pression d’environ 0,3 MPa et avec des temps de contact de l’ordre de 15 à 20 s.
L’optimisation du procédé consiste à réduire la quantité de sous-produits formés : les tétrachlorobutanes, le vinylcyclohexène, les monochlorobutadiènes, les trichlorobutènes et des lourds. Signalons qu’une augmentation de la température de réaction entraîne un accroissement de la proportion des produits de substitution...
Obtention des matières premières
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
BIBLIOGRAPHIE
-
(1) - JOHNSON (P.R.) - Polychloroprene Rubber. - Rubber Chemistry and Technology, vol. 49, p. 650-702.
-
(2) - HOLLIS (C.E.) - Chloroprene and Polychloroprene Rubbers. - Chemistry and Technology, p. 1030-1041 (1969).
-
(3) - EniChem Élastomères France - * - Notices techniques et brochure Relations entre les structures et les propriétés des polychloroprènes.
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.