Présentation
Auteur(s)
-
Lucien MARCOU : Ingénieur ESPCI (École supérieure de physique et chimie industrielles de Paris) - Président du comité technique « Agents de surface » du CEN (Comité européen de normalisation) - Président honoraire du Syndicat français des producteurs d’agents de surface et produits auxiliaires industriels (ASPA) - Ancien président du Comité international de la détergence (CID)
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
Le terme sulfonation désigne la réaction chimique permettant d’introduire un groupement sulfonique – SO3H dans une molécule, par liaison directe carbone-soufre [définition donnée dans les normes ISO 862 (1984) et EN ISO 862 (1995) – « Agents de surface. Vocabulaire »].
La sulfatation est la réaction chimique permettant d’obtenir un ester sulfurique. En pratique, on obtient un monoester sulfurique R—O—SO3M.
La chlorosulfonation, ou plus généralement les halosulfonations ainsi que la sulfoxydation, sont, par extension, considérées comme des sulfonations.
La sulfonation et la sulfatation ont pour but d’apporter ou d’améliorer la solubilité dans l’eau des molécules organiques ; elles sont utilisées pour la synthèse d’agents de surface anioniques ; la sulfonation permet aussi d’obtenir des intermédiaires de synthèse conduisant à des produits plus élaborés comme les phénols, par réactions dites d’échange (fusion alcaline).
VERSIONS
- Version archivée 1 de déc. 1982 par Pierre BOUVET
DOI (Digital Object Identifier)
Présentation
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
2. Sulfatation
La sulfatation a pour but d’apporter ou d’améliorer la solubilité dans l’eau de certaines molécules organiques ; elle est, entre autres, utilisée pour la synthèse d’agents de surface : alkylsulfates, alkyléthersulfates, sulforicinates...
2.1 Réaction de sulfatation directe
La sulfatation par SO3 gazeux est une réaction d’addition :
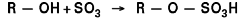
R étant un radical aliphatique.
Cette réaction est fortement exothermique. Elle est appliquée aux alcools gras (de C6 à C18 ), aux alcools condensés avec quelques molécules d’oxyde d’éthylène, ainsi qu’à tout autre condensat d’oxyde d’éthylène sur des molécules possédant au moins un hydrogène actif :
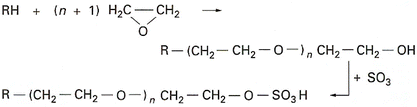
Dans le cas où R correspond à un radical aromatique substitué, cette réaction avec SO3 conduit, non seulement au sulfate, mais également à des dérivés de sulfonation du noyau aromatique. Afin d’éviter la formation de ces dérivés sulfonés, il est nécessaire d’utiliser d’autres agents de sulfatation, comme l’acide sulfamique.
HAUT DE PAGE2.2 Autres méthodes de sulfatation
2.2.1 Sulfatation par l’acide sulfamique H2NSO3
Cette méthode, beaucoup plus onéreuse que la sulfatation par SO3 n’est utilisée que pour la sulfatation de molécules comprenant un cycle aromatique et lorsqu’il faut éviter la formation de dérivés sulfonés. Ce procédé donne directement le sel d’ammonium du dérivé sulfaté ; il est utilisé, par exemple, pour la sulfatation...
Sulfatation
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.




