Présentation
Auteur(s)
-
Jean-Pierre CORRIOU : Ingénieur des Arts et Manufactures - Docteur ès Sciences - Maître-Assistant au Laboratoire de Chimie Nucléaire et Industrielle de l’École Centrale de Paris
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
Cet article a été initialement placé sous la responsabilité de M. T ivadar KIKINDAI, professeur à l’École Centrale de Paris, disparu avant d’en avoir entrepris la rédaction qui a été confiée ensuite à Jean-Pierre CORRIOU, son collaborateur.
Cet article présente les notions de base (définitions et relations fondamentales en thermodynamique chimique).
Il s’insère dans un ensemble qui constitue, avec les articles sur les Transferts de masse, l’une des pièces essentielles des Notions de base du présent traité Génie des procédés.
Le lecteur consultera donc également les articles suivants, consacrés à la thermodynamique chimique :
-
Diagrammes thermodynamiques Thermodynamique chimique- Diagrammes thermodynamiques ;
-
Équilibres thermodynamiques Thermodynamique chimique- Équilibres thermodynamiques.
Nous tenons à remercier M. Daniel GOURISSE, Directeur de l’École Centrale de Paris, d’avoir bien voulu créer les conditions d’exécution de ce travail par M. Corriou, membre du corps enseignant de cette École ; nous remercions également M. Francis DENNERY, Professeur de Thermodynamique à l’École Centrale, qui lui a apporté son parrainage et le précieux concours de sa compétence.
Bien que l’atmosphère ne soit pas l’unité légale de pression dans le Système International, cette unité sera couramment utilisée tout au long de cet article, car d’usage très répandu dans la profession.
VERSIONS
- Version archivée 1 de déc. 1984 par Jean-Pierre CORRIOU
- Version courante de févr. 2022 par Romain PRIVAT, Jean-Noël JAUBERT
DOI (Digital Object Identifier)
Présentation
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
3. Grandeurs et relations de la thermodynamique
3.1 Grandeurs fondamentales
3.1.1 Énergie interne, enthalpie
Pour un système échangeant du travail (δW 0) et de la chaleur (δQ ) avec le milieu extérieur au cours d’une transformation infiniment petite, le premier principe s’écrit :
avec :
- dU :
- une différentielle totale exacte puisque U est une fonction d’état.
Si le système est seulement soumis aux forces de pression et si la transformation est réversible, on a :
donc :
On introduit ainsi l’enthalpie :
qui est également une fonction d’état.
HAUT DE PAGE3.1.2 Entropie, potentiel chimique
D’après le deuxième principe, on a :
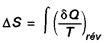
d’où, pour une transformation irréversible :
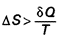
et pour une transformation...
Grandeurs et relations de la thermodynamique
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.












