Présentation
Auteur(s)
-
Richard PORTIER : Ingénieur de l’École Nationale Supérieure de Chimie de Paris - Professeur à l’Université Paris VI
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
Le calcul des systèmes polyélectroniques est rendu délicat par le fait qu’il n’existe pas de solutions analytiques exactes. Il convient donc d’utiliser des méthodes de résolutions approximatives et l’article Systèmes polyélectroniques modèles a permis de les présenter. Ainsi, l’approximation monoélectronique, pour laquelle chaque électron est décrit par une fonction qui ne dépend que de ses coordonnées, conduit à des équations dites de champ moyen où les répulsions interélectrons ne sont pas traitées de manière instantanée mais sont en fait moyennées. De plus, dans le cadre de cette approximation, les fonctions monoélectroniques de la molécule, les orbitales moléculaires, peuvent être développées sur une base formée par un nombre fini d’orbitales atomiques des atomes qui composent la molécule. Cette méthode a été testée sur l’ion moléculaire
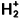 pour lequel nous connaissons des solutions exactes. C’est cette méthode que nous allons étendre au cas des molécules plus complexes. Les énergies des orbitales atomiques, c’est-à-dire des niveaux monoélectroniques des atomes, sont reportées sur le tableau 1.
pour lequel nous connaissons des solutions exactes. C’est cette méthode que nous allons étendre au cas des molécules plus complexes. Les énergies des orbitales atomiques, c’est-à-dire des niveaux monoélectroniques des atomes, sont reportées sur le tableau 1.
DOI (Digital Object Identifier)
Présentation
Article inclus dans l'offre
"Physique Chimie"
(205 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
1. Molécule d’hydrogène
La molécule d’hydrogène constitue le plus simple des systèmes moléculaires pour lequel une résolution analytique exacte est impossible. Elle représente de ce fait un système polyélectronique modèle pour tester la méthode des orbitales moléculaires développées sur une base d’orbitales atomiques. Cependant, nous développerons également, dans un premier temps, la méthode de Heitler et London.
1.1 Hamiltonien du système
La molécule d’hydrogène, H2 , comprend quatre particules en interaction : deux électrons et deux protons. Avec l’approximation de Born-Oppenheimer, le problème se réduit à l’étude de deux électrons dans le champ des deux noyaux considérés comme fixes. La distance internucléaire devient alors un paramètre comme pour le calcul de
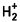 . Le hamiltonien du système, en adoptant les unités atomiques, s’écrit :
. Le hamiltonien du système, en adoptant les unités atomiques, s’écrit :
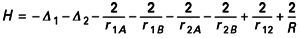
avec les notations de la figure 1.
Les deux premiers termes du hamiltonien constituent l’énergie cinétique des électrons, les autres termes représentent les interactions coulombiennes entre particules chargées.
Le hamiltonien du système est donc exact, mais la difficulté vient de ce qu’il n’y a pas de solution analytique pour l’équation de Schrödinger :
Il faut donc chercher des solutions approchées et nous allons développer deux méthodes.
HAUT DE PAGE1.2 Méthode de Heitler et London (1927)
Quand les deux atomes sont à grande distance, il n’existe plus d’interactions coulombiennes entre eux et le hamiltonien du système se réduit à la somme de deux hamiltoniens monoélectroniques, chacun étant celui d’un atome...
Molécule d’hydrogène
Article inclus dans l'offre
"Physique Chimie"
(205 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
Article inclus dans l'offre
"Physique Chimie"
(205 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.




