Présentation
RÉSUMÉ
Les propriétés thermodynamiques des composés organiques sont rassemblées en un tableau donnant, pour chaque composé, sa formule brute, son nom, son état, son enthalpie standard de formation, son entropie standard et sa capacité thermique, toutes ces grandeurs étant tabulées à 25 degrés Celsius. Les enthalpies de combustion, et les enthalpies libres de formation n’apparaissent pas, mais les calculs sur la base des valeurs tabulées sont présentés. Les valeurs relatives aux composés minéraux les plus souvent rencontrés dans les réactions organiques ont été ajoutées. En présence de données calculées et de données expérimentales, les dernières ont été retenues sauf lorsqu'elles s'écartaient trop des données calculées, qui ont dans ce cas été considérées plus réalistes.
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleAuteur(s)
-
Pierre PERROT : Professeur émérite - Laboratoire de métallurgie physique - Université des sciences et technologies de Lille
INTRODUCTION
Les propriétés thermodynamiques des composés organiques sont rassemblées en un seul tableau donnant, pour chaque composé, sa formule brute, son nom, son état, son enthalpie standard de formation, son entropie standard et sa capacité thermique, toutes ces grandeurs étant tabulées à 25 ˚C. Dans ce tableau, nous avons choisi de privilégier le nombre de composés présentés aux dépens de données redondantes qu'il est possible de calculer, si besoin est, à partir des seuls éléments y figurant. C'est ainsi que nous n'avons présenté ni les enthalpies de combustion, ni les enthalpies libres standards de formation, mais nous expliquons comment les calculer simplement à partir des valeurs tabulées. En revanche, nous avons introduit les valeurs relatives aux composés minéraux les plus souvent rencontrés dans les réactions organiques. Ces composés sont au nombre d'une trentaine, ce qui, au prix d'un alourdissement du tableau de 2 %, présente l'avantage de le rendre autosuffisant. En plus de cet effort pour éviter les redondances, nous avons dû faire des choix, car il ne nous a pas été possible d'introduire toutes les valeurs dont nous disposions. En premier lieu, nous avons évité, à de très rares exceptions près, les composés pour lesquels il nous manquait une ou deux données. Ensuite, de façon parfois subjective, nous avons éliminé les composés pour lesquels les données nous semblaient aberrantes. Lorsque nous disposions de données calculées et de données expérimentales, nous avons privilégié ces dernières sauf lorsqu'elles s'écartaient trop des données calculées, auquel cas nous avons pensé que les résultats calculés étaient plus réalistes. En effet, l'évolution monotone des propriétés le long d'une série peut fournir une indication précieuse sur la crédibilité de certaines grandeurs. Nous présentons rapidement ci-dessous le tableau et donnons quelques exemples de la manière dont il peut être utilisé : calcul d'une enthalpie de combustion, d'une enthalpie libre de réaction, d'une constante d'équilibre. Un exposé plus détaillé peut être consulté en [K 610].
VERSIONS
DOI (Digital Object Identifier)
Présentation
Article inclus dans l'offre
"Caractérisation et propriétés de la matière"
(115 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
5. Entropie de réaction
L'entropie standard de la réaction
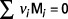 est calculée par :
est calculée par :
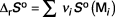
Exemple : appliquée à la réaction de déshydrogénation de l'éthylbenzène, la méthode donne :
Si la réaction ne se fait pas à 25 ˚C, il est nécessaire de faire intervenir les capacités thermiques :
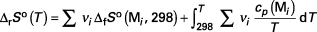
Exemple : appliquée à la réaction de déshydrogénation de l'éthylbenzène à 727 ˚C (1 000 K), la méthode donne :
Entropie de réaction
Article inclus dans l'offre
"Caractérisation et propriétés de la matière"
(115 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
BIBLIOGRAPHIE
-
(1) - STULL (D.R.), WESTRUM Jr. (E.F.), SINKE (G.C.) - The chemical thermodynamics of organic compounds - . J. Wiley & Sons, New York (865 pages, 1 656 références. 740 substances tabulées plus 3 700 données à 298 K) (1969).
-
(2) - COX (J.D.), PILCHER (G.) - Thermochemistry of organic and organometallic compounds - . Academic Press, New York (636 pages, 2 000 substances) (1970).
-
(3) - PEDLEY (J.B.), NAYLOR (R.D.), KIRBY (S.P.) - Thermochemical data of organic compounds - . Chapman & Hall, New York (Reprend et complète les données de ) (1986).
-
(4) - STEPHENSON (R.M.), MALANOWSKI (S.) - Handbook of the thermodynamics of organic compounds - . Elsevier, New York (552 pages) (1987).
-
(5) - WEAST (R.C.), GRASSELI (J.G.) - CRC Handbook of data on organic compounds - . 2nd Ed. CRC Press, Boca Raton, FL (1989).
-
(6)...
Article inclus dans l'offre
"Caractérisation et propriétés de la matière"
(115 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.