Développée depuis les années 1970, la cryomicroscopie électronique a connu ces dernières décennies de grandes avancées grâce notamment à l’évolution de la technique et de l’analyse d’image. Mais à quoi sert-elle exactement ? Quelle est son utilisation en France ? Explications.
La cryomicroscopie électronique (cryo-ME) a fait l’objet d’une couverture médiatique en 2017. Le prix Nobel de chimie a été décerné à trois scientifiques pour leurs travaux de développement de la technologie : Jacques Dubochet, Joachim Frank et Richard Henderson. Cette technique d’imagerie utilise un faisceau d’électrons pour réaliser, à partir d’échantillons biologiques (protéines, ADN, virus, bactéries, cellules) cryogénisés à -180°C, des modèles 3D à de hautes résolutions, jusqu’à des détails atomiques.
Dans un article publié en avril 2021 dans la revue Médecines Sciences, Daniel Lévy, directeur de recherche en biologie à l’Institut Curie, et ses co-auteurs, détaillent les avancées de la cryomicroscopie électronique. Nous avons échangé avec lui pour comprendre l’impact de ces avancées, mais également les applications de cette technologie.
Techniques de l’Ingénieur : Quelles sont les évolutions de la cryomicroscopie électronique ?
Daniel Lévy : La cryomicroscopie est une technique d’imagerie du vivant qui s’est développée depuis les années 1970 et qui a vécu une révolution forte à partir de 2014. Ces dernières années, les microscopes et détecteurs sont également plus performants, notamment la qualité du faisceau d’électrons, des lentilles électromagnétiques plus stables, des diaphragmes automatisés, ou encore des caméras à détection directe d’électrons.
En parallèle, un développement important a été réalisé sur l’analyse des images. On va pouvoir à la fois regarder des composants cellulaires présentant des mutations ou des dysfonctionnements à l’origine d’une maladie à des résolutions que l’on n’avait pas auparavant. Ce qui est très utile pour comprendre le vivant, à la fois dans la recherche académique, mais également pour des applications biomédicales.
Pourquoi faut-il combiner la cryogénie à l’imagerie pour analyser le vivant ?
Pour faire des images les plus précises possibles, on va figer l’échantillon biologique dans une couche mince de glace vitreuse, transparente aux électrons. Cette technique permet d’éviter la formation de cristaux de glace pouvant abîmer les structures. L’échantillon doit ensuite être maintenu à -180°C pendant l’observation.
Pouvez-vous nous donner des exemples d’applications ?
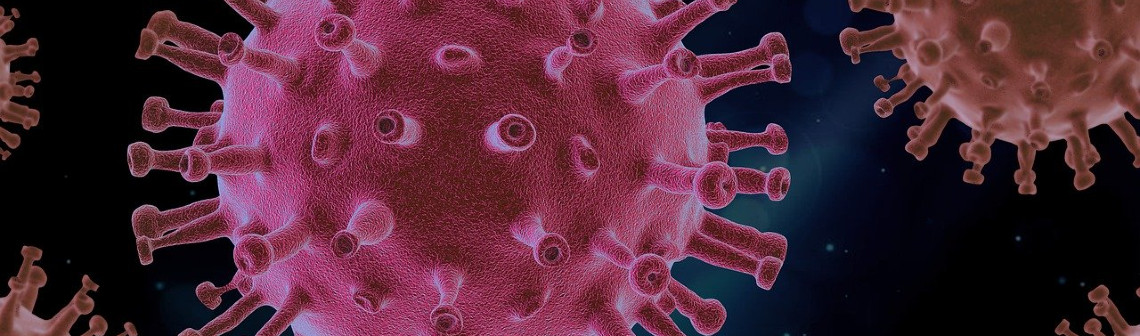
Prenons l’image du virus du Covid-19 que l’on voit dans les médias : une boule avec des picots. La protéine de surface est celle qui va reconnaître un récepteur dans une cellule et y entrer. Lorsqu’on parle de variant, cela signifie qu’une mutation d’un acide aminé – une partie de la protéine – va se fixer de manière plus efficace sur une cellule humaine, et va donc entrer plus facilement. Cette mutation est visualisée par cryomicroscopie électronique.
Autre exemple : depuis longtemps, on connaît l’existence des protéines membranaires réceptrices de toutes nos sensations (douleur, goût, odorat). Lorsqu’elles sont déréglées, elles sont la source de maladies neurodégénératives. Cependant, nous n’avions pas idée de la façon dont elles s’organisaient dans l’espace et comment on pouvait agir dessus. Grâce à la cryomicroscopie, nous avons désormais des modèles dans l’espace en 3 dimensions, où l’on voit très bien à quel endroit le médicament intervient dans la protéine. Soit un activateur qui va pouvoir entrer, soit un inhibiteur qui va pouvoir la bloquer.
Cela permet de comprendre le fonctionnement et l’action d’un médicament ?
Oui, et de concevoir de nouveaux médicaments. Avant que le vaccin ARN soit injecté à des patients par exemple, on réalise des images de la formulation vaccinale pour voir à quoi cela ressemblait. Dans le cas du vaccin contre le Covid-19, ce n’est pas un simple ARN car il est englobé dans une capsule lipidique et compacté pour pouvoir entrer dans les cellules. Et pour être sûr qu’il soit bien compacté, on fait des images de cryomicroscopie.
Quelles sont les limites de l’instrument ?
Il y avait un tas de limitation technologique pour observer des protéines humaines, par des approches autres que la cryomicroscopie. Aujourd’hui, il est possible de les regarder à des résolutions quasi atomiques. Cependant, sur les aspects d’analyse d’image où on doit passer beaucoup de temps pour le traitement, cela reste encore compliqué à cause d’un mauvais rapport signal sur bruit. En d’autres termes, le signal des détails dans l’image est très faible. On va donc utiliser différentes approches algorithmiques pour faire ressortir ces détails. Cela stimule beaucoup de recherches dans la communauté des mathématiques appliquées pour faire cette approche de reconnaissance des signaux, via le machine learning et le deep learning. C’est ce qui est en cours pour faire évoluer la technologie.
De plus, depuis cinq ans, la cryomicroscopie était réservée à des experts. Aujourd’hui, ils sont rejoints par des professionnels de la pharmacologie, de la biologie fondamentale, de la recherche agronomique – pour les protéines impliquées dans la résistance aux insecticides par exemple –, des mathématiques appliquées ou encore de la physique. L’un des objectifs est que l’instrument devienne plus accessible en termes de compréhension, que les scientifiques n’aient plus à se soucier de la façon dont la technologie fonctionne. Pour le moment, les gens qui réalisent de bonnes images sont des experts. Ceux qui interprètent les images aussi.
Quels sont les autres objectifs ?
Les autres objectifs sont les applications : visualiser pour comprendre le fonctionnement du maximum de protéines impliquées avec des applications biomédicales, industrielles, agronomiques, fondamentales… Grâce à la cryomicroscopie, on a pu comprendre à l’échelle atomique comment se formaient les plaques amyloïdes dans les maladies neurodégénératives du type Alzheimer, à partir d’une biopsie de patient. On est donc sur de l’analyse directe d’échantillons de patient et non in vitro. Cela permet d’aller chercher, dans les tissus de patients, les protéines responsables de la maladie. Alors qu’habituellement, dans un laboratoire, on crée artificiellement une protéine avec différentes approches et on l’étudie. On ne va pas extraire les protéines des patients. Désormais avec la cryomicroscopie, c’est possible. On sera plus proche du patient.
La technologie est-elle bien développée en France ?
La France a pris beaucoup de retard dans cette technique. Mais elle mène des actions pour rattraper ce retard. Il y a environ 250 cryomicroscopes à très haute résolution dans le monde, et seulement 3 en France et d’autres sont prévus. Les laboratoires pharmaceutiques, comme Pfizer, Novartis et Aztrazeneca, s’équipent. Les cryomicroscopes sont des instruments très coûteux, entre 5 et 10 millions d’euros. En revanche, l’impact économique de la compréhension de protéines à impact biomédical est beaucoup plus important.
La cryomicroscopie n’est pas une expertise française ?
Non, la cryomicroscopie a avant tout été développée par des laboratoires japonais, anglais, allemand et également américain. Et les principaux fabricants de cryomicroscopes sont l’Américain ThermoFischer et le Japonais Jeol, le premier détenant environ 90 % du marché. Ce qui pose problème car il n’y a pas de mise en concurrence possible… Au départ, il y a une trentaine d’années, il y avait deux fabricants, dont l’un était Philips. Mais il a été racheté par l’américain FEI, puis ThermoFischer.
Nous avons de très bons laboratoires en cryomicroscopie en France, mais peu. Ils sont beaucoup plus nombreux dans les autres pays.
En quoi est-ce intéressant pour un ingénieur de travailler sur ce type d’instrument ?
Même si l’application est biologique, l’instrument reste un instrument de physique. Il permet donc à des ingénieurs, qui ont des formations en physique, optique, imagerie ou encore informatique, de travailler sur ces technologies.














Réagissez à cet article
Connectez-vous
Vous avez déjà un compte ? Connectez-vous et retrouvez plus tard tous vos commentaires dans votre espace personnel.
Vous n'avez pas encore de compte ?
Inscrivez-vous !