Présentation
Auteur(s)
-
François NICOLAS : Ingénieur de recherche à la Compagnie générale des matières nucléaires (COGEMA)
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
Le fluor est produit par électrolyse de l’acide fluorhydrique contenu dans le sel fondu anhydre KF, 2 HF à une température voisine de 100 ˚C.
Sa principale utilisation se situe dans l’industrie nucléaire lors de la synthèse de l’hexafluorure d’uranium, forme sous laquelle l’uranium est enrichi en son isotope fissile (U235) par diffusion gazeuse ou ultracentrifugation.
Le fluor sert également à la synthèse de composés inorganiques tels que SF6 (diélectrique), WF6, ClF3, IF5.
DOI (Digital Object Identifier)
Présentation
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
2. Fiche produit
2.1 Propriétés physico-chimiques
Dans les conditions normales de température et de pression, le fluor est un gaz jaune pâle à odeur piquante. De numéro atomique Z = 9, il occupe la case voisine du néon dans la classification périodique où il est le premier des halogènes.
Il fut découvert, il y a un peu plus d’un siècle, par le chimiste français Henri Moissan, lors de l’électrolyse d’une solution de fluorure de potassium dans le fluorure d’hydrogène anhydre.
La masse atomique relative du fluor est 18,9984032 (IUPAC 1993).
La valeur de l’énergie de la liaison
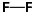 est de 158,3 kJ/mol. Cette faible valeur contribue à donner aux réactions du fluor un caractère très exothermique.
est de 158,3 kJ/mol. Cette faible valeur contribue à donner aux réactions du fluor un caractère très exothermique.
Les données thermodynamiques du fluor sont les suivantes :
-
enthalpie de fusion 509 J . mol−1
-
enthalpie de vaporisation à 85,0 K 6 509 J . mol−1
-
entropie standard 203 J . mol−1 . K−1
-
capacité thermique molaire standard 31,3 J . mol−1 . K−1
état standard : pression da 1,013 × 105 Pa et température de 25˚ C ou 298,2 K.
Les propriétés physiques les plus importantes sont rassemblées dans le tableau 2.
Le potentiel réversible d’une électrode à fluor, dans les conditions standards, trouvé égal à 2,85 ± 0,04 V, a été calculé à partir de l’énergie libre de formation de HF en milieu aqueux, car il est inaccessible expérimentalement . Du point de vue pratique, on se réfère plutôt à la tension minimale de décomposition de HF en milieu fluorure fondu....
Fiche produit
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
BIBLIOGRAPHIE
-
(1) - LATIMER (W.) - The potential of the fluorine electrodes from thermal data - . J. Am. Chem. Soc. 48 p. 2868-9 (1926).
-
(2) - DEVILLIERS (D.), LANTELME (F.), CHEMLA (M.) - Étude de la tension de décomposition de HF sur électrode de carbone dans un bain 2 HF, KF - . J. Chim. Phys., Phys. Chim. Biol. 76 no 5 p. 428-32 (1979).
-
(3) - ULLMANN’S - Encyclopedia - , vol. A11 p. 293-308 (1988).
-
(4) - Fluor - . Fiche toxicologique no 203 INRS (1992).
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.













