Présentation
Auteur(s)
-
François NICOLAS : Ingénieur de recherche à la Compagnie générale des matières nucléaires (COGEMA)
Lire cet article issu d'une ressource documentaire complète, actualisée et validée par des comités scientifiques.
Lire l’articleINTRODUCTION
Le fluor est produit par électrolyse de l’acide fluorhydrique contenu dans le sel fondu anhydre KF, 2 HF à une température voisine de 100 ˚C.
Sa principale utilisation se situe dans l’industrie nucléaire lors de la synthèse de l’hexafluorure d’uranium, forme sous laquelle l’uranium est enrichi en son isotope fissile (U235) par diffusion gazeuse ou ultracentrifugation.
Le fluor sert également à la synthèse de composés inorganiques tels que SF6 (diélectrique), WF6, ClF3, IF5.
DOI (Digital Object Identifier)
Présentation
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
1. Procédé
1.1 Principe
Le fluor est préparé par électrolyse du fluorure d’hydrogène anhydre, rendu conducteur par l’addition d’un fluorure métallique. Les producteurs industriels utilisent le sel fondu de composition voisine de KF, 2 HF à une température comprise entre 85 et 105 ˚C.
Dans ce milieu, la décomposition du fluorure d’hydrogène s’effectue à un potentiel minimal de 2,9 V selon la réaction :
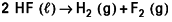
avec
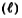 liquide et (g) gaz.
liquide et (g) gaz.
Le sel fondu est préparé par réaction exothermique du sel commercial de Frémy (KF, HF) et de fluorure d’hydrogène anhydre. Du fluorure de lithium à raison de 2 à 3 % est ajouté au bain pour éviter la polarisation des anodes lors de l’électrolyse.
La consommation de HF pendant l’électrolyse, due à la production de fluor et à l’évaporation, est compensée par un apport constant. Il faut approximativement 1,1 t de HF pour produire 1 t de fluor.
HAUT DE PAGE1.2 Description de l’installation. Conditions opératoires
-
Le schéma type d’une unité de production est présenté figure 1.
-
Cellule d’électrolyse
La cuve d’électrolyse, de dimensions approximatives : 3 × 0,9 × 0,9 m, est construite en Monel (alliage à 70 % nickel – 30 % cuivre), ou en acier lorsque celle-ci fonctionne comme cathode.
Les anodes, au nombre de 24 à 44, sont en carbone poreux non graphité et les cathodes en acier. Le séparateur des gaz hydrogène et fluor est en Monel.
À l’arrêt de l’électrolyseur, le maintien en température du bain est assuré par l’injection de vapeur dans des serpentins en Monel entourant la cathode. En régime de fonctionnement, une circulation d’eau est nécessaire.
Les...
Procédé
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.
BIBLIOGRAPHIE
-
(1) - LATIMER (W.) - The potential of the fluorine electrodes from thermal data - . J. Am. Chem. Soc. 48 p. 2868-9 (1926).
-
(2) - DEVILLIERS (D.), LANTELME (F.), CHEMLA (M.) - Étude de la tension de décomposition de HF sur électrode de carbone dans un bain 2 HF, KF - . J. Chim. Phys., Phys. Chim. Biol. 76 no 5 p. 428-32 (1979).
-
(3) - ULLMANN’S - Encyclopedia - , vol. A11 p. 293-308 (1988).
-
(4) - Fluor - . Fiche toxicologique no 203 INRS (1992).
Article inclus dans l'offre
"Opérations unitaires. Génie de la réaction chimique"
(370 articles)
Actualisée et enrichie d’articles validés par nos comités scientifiques.
Quiz, médias, tableaux, formules, vidéos, etc.
Opérationnels et didactiques, pour garantir l'acquisition des compétences transverses.
Un ensemble de services exclusifs en complément des ressources.













